|
宋安東,馮新軍,謝慧,王風芹
(河南農業(yè)大學 生命科學學院 農業(yè)部農業(yè)微生物酶工程重點實驗室,鄭州 450002)
摘要:論述了合成氣制取乙醇的必要性,重點對以合成氣為原料制取燃料乙醇的化學催化法(費托合成法)和厭氧發(fā)酵法兩種技術的優(yōu)缺點進行對比分析,指出了利用合成氣通過厭氧發(fā)酵技術來生產乙醇具有顯著的優(yōu)勢,同時也提出了合成氣厭氧發(fā)酵制取乙醇技術中存在的問題和建議。
乙醇是一種重要的有機原料,被廣泛用作有機溶劑、消毒劑、飲料、食品添加劑和防腐劑等,是一種不含S及灰分的清潔能源,被認為是替代汽油的最佳燃料之一,每千克乙醇完全燃燒時約能放出30MJ的熱量。將一定量的燃料乙醇加入汽油后,混合燃料的含氧量增加,辛烷值提高,能夠降低汽車尾氣中有害氣體的排放量[1]。
美國能源部規(guī)劃2020年燃料乙醇年產6000~9000萬t,2050年年產1.4億t,占總消費的1/3[2]。
我國“十二五”規(guī)劃的燃料乙醇產量為500萬t,《國家中長期科學和技術發(fā)展規(guī)劃綱要》提出,到2020年燃料乙醇用量擴大到1000萬t。截至目前,國家發(fā)展和改革委員會批準的安徽、河南、吉林、黑龍江、廣西地區(qū)的5個燃料乙醇企業(yè)總設計產量為164萬t,2010年的產量為175萬t,距“十二五”規(guī)劃目標還有325萬t的缺口。
乙醇的生產方法包括糧食發(fā)酵法、木材水解法、乙烯直接水合法、乙烯間接水合法、乙醛加氫法、CO(CO2)和H2的羰基化學合成法等[3],目前主要采取的是糧食發(fā)酵法和氣體化學合成法。發(fā)酵法生產的乙醇占全球乙醇總量的95%以上。傳統(tǒng)的糧食發(fā)酵法存在很多問題,如技術陳舊、原料耗費大、生產成本高、廢渣廢水處理比較困難等,難以保證國民經濟快速發(fā)展對能源的需求。按照《國家中長期科學和技術發(fā)展規(guī)劃綱要》和農業(yè)部《農業(yè)生物質能產業(yè)規(guī)劃(2007~2015)》中提出的“不與人爭糧、不與糧爭地”的指導方針,開展新型乙醇生產技術研究與開發(fā)日趨顯得重要。利用合成氣制取乙醇作為一個重要的發(fā)展領域越來越受到關注。
1利用合成氣轉化成乙醇
合成氣是由煤、重油或天然氣生產以H2與CO為主要成分的原料氣。合成氣的原料來源范圍極廣,生產方法甚多,導致其組成(體積分數(shù))有很大差別:H232%~67%、CO10%~57%、CO22%~28%、CH40.1%~14%、N20.6%~23%[4-5]。
我國有豐富的合成氣資源。石油石化企業(yè)在生產活動中會產生大量的溫室氣體,這些溫室氣體主要產生于石油天然氣勘探開發(fā)、煉油與化工和油氣儲運3個環(huán)節(jié)[6]。2009年,中國煉廠規(guī)模超過了120百萬公噸(MMT),而由此產生的煉廠干氣約為5.5MMT[7]。煉廠干氣主要組分為H2、CO、CO2、O2、CH4、C2H4、C2H6、C3H8及微量S、重金屬等;H2、CO、CO2經過一定的精煉、濃縮可達到45%左右[8]。
H2、CO、CO2等正好是合成氣的主要成分。另外,據(jù)初步統(tǒng)計,中國每年排放的焦爐煤氣約為400億m3,如果加以利用,每年可以生產1300萬t乙醇,能夠產生巨大的經濟效益和社會效應。
美國、瑞典、日本等國對利用合成氣生產液體燃料如生物油、二甲醚、乙醇、甲醇、丁醇等進行了大量的研究[9];在國內,中國科技大學、浙江大學、中國科學院廣州能源所、中國科學院大連化學物理研究所和華東理工大學等單位也進行了相應的研究,并建起了相應的示范裝置[9],目前還停留在實驗室階段。
利用合成氣制備乙醇具有顯著優(yōu)點:①原料來源廣,原料合成氣可以來自固體(煤、焦、生物質)、氣體(天然氣、乙炔尾氣、焦爐煤氣)和液體(輕油、重油、焦油)等。利用合成氣生產乙醇可以降低糧食消耗,實現(xiàn)國家的長治久安。②環(huán)境友好,利用CO2合成乙醇,使乙醇的生產與CO2的消耗形成閉合循環(huán),從而實現(xiàn)CO2減排,減緩地球溫室效應[3]。
利用合成氣制乙醇主要有2條途徑:一是化學催化法,即費托合成法(FT);二是微生物厭氧發(fā)酵法(AF)。下面對這2種技術路線進行綜述并分析。
2 FT法制乙醇主要優(yōu)缺點
2.1 FT制乙醇的優(yōu)點
FT制乙醇的優(yōu)點在于:①勞動生產率高,F(xiàn)T法是糧食微生物發(fā)酵法的50倍;②產品成本低,F(xiàn)T法是糧食微生物發(fā)酵法的1/10;③基建費用低,F(xiàn)T法是糧食微生物發(fā)酵法的1/2[3]。
關于FT法制取乙醇的研究,主要集中在合成氣生產乙醇的基礎研究與工程示范領域,特別是對于高性能、耐受性催化劑的開發(fā)以及對合成過程和工藝條件的優(yōu)化。
FT法制乙醇的關鍵是選擇性能較高、催化性能較好、耐受性能較強、穩(wěn)定性強的催化劑。國內外對催化劑的選擇、制備和應用以及催化劑助劑的選擇等方面進行了研究,主要集中在銠基催化劑(如Rh/SiO2催化劑和擔載型銠催化劑)和非銠基催化劑(如K-Mo-Co/活性炭催化劑、Cu-Zn-Fe/K固體催化劑、CuCoMn催化劑、Cu/Al2O3、Mo2-Co2-K硫化鉬基催化劑)的選擇、制備和性能研究[3]以及催化條件包括催化劑用量、合成條件(溫度、壓力和空速)等上面,目的在于提高乙醇等低碳醇合成過程的單程轉化率、合成氣的選擇性和醇產率[10]。
目前,取得了一定的研究結果,乙醇的選擇性可以達到75%以上,乙醇產率可以達到13%~18%以上,可以實現(xiàn)1000h以上的連續(xù)運轉[3]。
為了改善催化劑性能提高目的產物的選擇性,Haider等[11]研究了各種助劑對催化性能的影響。
加入Fe、Ir、Ti等金屬增強加氫能力,加入Mn、Sc、V、Zr等金屬增強CO離解能力,加入K、Li等金屬抑制加氫能力。即使如此,單獨提高乙醇選擇性仍很困難。
2.2FT制乙醇的局限性和弊端
盡管對FT法制乙醇進行了大量研究,取得了一定的進展,但該技術仍有很大的局限性和弊端,主要表現(xiàn)在以下幾方面。
1)選擇性低。FT法制乙醇的產物很雜,其產物以乙醇為主,還有可以生成從甲醇到C5、C6的醇類混合物,還可產生如乙酸、乙醛、乙酸乙酯、乙酸等其他C2含氧化合物。從合成氣出發(fā),無論是生成烴類,還是生成醇類,高選擇性地生成C2物種(乙烷或者乙醇)都沒有實現(xiàn)工業(yè)化過程。即目前無論是從合成氣制烴類還是制醇,利用現(xiàn)有的催化劑高選擇性地把碳鏈增長過程停止在C2這一步仍然具有相當大的困難,這是最大的缺陷,也是高選擇性催化劑和催化反應過程研究的重點和難點。為了提高反應速率,還需要適當提高反應溫度,但是伴隨著溫度升高,會相應發(fā)生一些副反應,抑制了乙醇的產生。為了促使反應向主反應方向進行,尋找一種選擇性能較高、催化性能較好的催化劑非常必要[3]。
2)反應溫度高,壓力高。FT法制乙醇通常反應溫度為315℃、反應壓力為8.2MPa。即便是采用最新發(fā)展起來的綠色催化技術,如將Ru催化劑加工到2.4nm使費托合成的反應溫度降低100℃而活性達到傳統(tǒng)Ru催化劑(200℃)的2~5倍[12],此時的反應溫度仍然在100~150℃以上,依然比微生物發(fā)酵所需要的溫度要高得多。這導致化學法合成乙醇熱效率損失大,加熱成本大,能耗高,反應裝備要求苛刻。
3)催化劑制備的條件苛刻。催化劑需要在高溫下焙燒數(shù)小時,溫度在250~500℃。
4)催化劑的成本高,工業(yè)化生產難以實現(xiàn)。這些催化劑一般以貴金屬為主要活性成分,如銠基催化劑等,開發(fā)非銠基或減少銠的含量是解決這一過程面向應用的重點和難點。Kharas等[13]研究了用鈷鉬硫作催化劑從合成氣來生產乙醇,但仍需要在325~340℃下反應,得到的產物是混合醇,且乙醇產量很低。
5)催化劑的生產和使用會出現(xiàn)嚴重的環(huán)境污染。催化劑生產大多會產生廢渣和廢水,同時催化劑中重金屬的流失等問題會出現(xiàn)嚴重的環(huán)境污染,廢水等的治理難度大[3]。
6)動力消耗高,F(xiàn)T法制乙醇的動力消耗是糧食微生物發(fā)酵法的4倍[3]。
7)合成氣要求高,需要凈化。乙醇合成過程中,對原料氣的凈化要求十分嚴格。原料氣的成分比較復雜,除了多種類型的硫和氨,還含有焦油、酚類、苯、萘、不飽和烯烴甚至氯類等雜質,這些雜質在后續(xù)的氣體轉化和乙醇合成中會影響催化劑的活性,尤其是由無機硫和有機硫組成的混合硫化物是氣體轉化和乙醇合成催化劑的有毒物質,會導致轉化和合成催化劑永久性中毒失活。因此,必須對原料氣進行深度凈化,如使用Fe2SO4和鈷鉬催化劑脫硫的干法脫硫或多級脫硫工藝進行脫硫,使總硫不大于0.1×10-6mg/m3。另外,用于合成乙醇的合成氣需要控制在一定比例范圍內,H2與CO的最佳摩爾比為2∶1,有CO2存在時,H2與COx的摩爾比值控制在3~5之間[3]。
8)合成氣中的CH4不能利用,導致原料氣利用率低,乙醇產率低。化學法制乙醇中,合成氣中還會含有少量的CH4(一般體積分數(shù)0.2%~1.5%)不參與乙醇的合成,稱之為惰性氣體。隨著反應進行,CH4含量會逐漸增多,從而使CO、CO2與H2的有效分壓降低,對合成反應不利,同時會增加壓縮機的動力消耗。在化學法合成氣制乙醇中需要控制CH4的量[3]。然而,生物法合成氣制乙醇中,CH4可以被微生物代謝最終也轉化成乙醇,乙醇產率高。
9)設備磨損大。合成乙醇反應需要在盡可能低的溫度、較高的壓力和較高的H2/COx體積比條件下進行。但是,過高的H2/COx體積比會浪費H2,過高的壓力不僅不能明顯提高轉化率,反而會增大設備的磨損[3]。
鑒于FT法制乙醇技術的缺點,利用現(xiàn)代生物技術手段,發(fā)展新型的合成氣發(fā)酵法制乙醇技術勢在必行。
3合成氣厭氧發(fā)酵(AF)生產乙醇
國內外對利用合成氣AF法制生產乙醇的微生物、代謝途徑、生產工藝和產業(yè)化研發(fā)等進行了一定的研究。
3.1合成氣發(fā)酵生產乙醇微生物研究
從20世紀80年代開始,科研工作者從動物糞便如雞糞[14]、兔糞[15]、農業(yè)瀉湖[16]、下水道污泥[14]、煤漿[14]等物質中篩選出了能夠利用合成氣生產乙醇的微生物,研究和報道最多的是Clostridi-um ljungdahlii、Clostridium carboxidivorans P7等[17],這些菌種都是嚴格的厭氧菌,能夠耐高濃度CO2、CO、NOx、SOx等氣體組分。最適生長溫度一般在37℃左右,適宜乙醇代謝的pH為4.0~7.5。近幾年,科研人員發(fā)現(xiàn)Clostridium thermoaceticum和Moorellasp.HUC22-1等嗜熱菌也可以利用合成氣發(fā)酵生產乙醇,這2種菌利用合成氣生產乙醇的最適溫度都在55℃左右[18]。
3.2合成氣發(fā)酵基本過程和代謝途徑研究
微生物利用合成氣AF法制燃料乙醇的代謝途徑已經有過很多報道[19-22],現(xiàn)在已經證明微生物利用H2、CO、CO2等發(fā)酵合成乙醇和乙酸以及其他副產物的實現(xiàn)是通過厭氧乙酰輔酶A(acetyl-CoA)途徑(圖1)[19]。沒有O2或其他氧化劑參與的厭氧代謝與好氧代謝相比,更能夠有效地保留底物合成氣中的化學能,因為在厭氧代謝過程中,沒有因電子流到分子氧或者氧化劑中造成的損失,這為以合成氣為原料生產燃料和化學品提供了樂觀的轉化途徑。厭氧乙酰輔酶A途徑是在絕對厭氧條件下進行的一種不可逆、非循環(huán)反應途徑[23]。
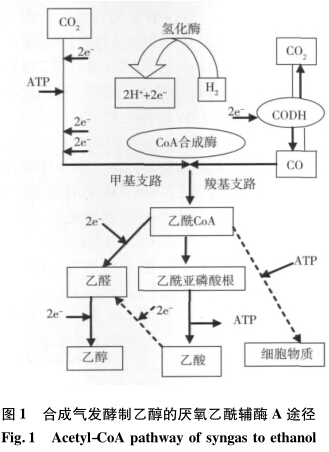
CO、CO2通過乙酰輔酶A途徑的甲基支路、羧基支路,消耗ATP,通過乙酰輔酶A合成酶(acetylcoenzyme A synthetase,ACS)和CO脫氫酶(carbonmonoxide dehydrogenase,CODH)的作用合成乙酰輔酶A。乙酰輔酶A隨后被逐步還原成乙醇、乙酸,或者用來合成細胞物質。氫化酶(hydrogenase,H2ase)、CODH、ACS、乙醛脫氫酶(aldehyde dehydro-genase,ALDH)、乙醇脫氫酶(alcoholde hydrogenase,ADH)、磷酸轉乙酰酶(phosphotransacetylase,PTA)和乙酸激酶(acetate kinase,AK)是代謝關鍵酶。
H2ase氧化H2產生還原力,對于后續(xù)的代謝非常重要,進而影響碳轉化率。CODH可以氧化CO形成CO2,還可以與乙酰輔酶A合成酶共同作用,催化前面代謝中獲得的甲基、羧基和CoA基團合成乙酰輔酶A。ACS催化CO、CO2和H2進行甲基支路和羧基支路反應,形成乙酰CoA,乙酰CoA是微生物厭氧發(fā)酵代謝產生乙醇的直接底物,該物質的積累多少直接影響著乙醇的產量。ALDH和ADH是從乙酰輔酶A到乙醇代謝途徑中的2種關鍵酶。PTA和AK是從乙酰輔酶A到乙酸代謝途徑中的2種關鍵酶。
3.3合成氣制乙醇發(fā)酵工藝及產業(yè)化進展
微生物利用合成氣AF法制燃料乙醇已經有了很多的研究,涉及影響生物質氣化、發(fā)酵過程以及后期的物質提煉等各個因素,以求提高乙醇產率,符合工業(yè)化的需要。
Klasson等[24]和Phillips等[4]分別在不同的菌株、培養(yǎng)基、合成氣成分以及操作條件(氣體流率、液體流率、氣相停留時間、液相停留時間、液體稀釋率、攪拌速率等)下,對乙醇發(fā)酵情況做了詳細的試驗研究,包括對細胞的出口濃度、乙酸和乙醇的出口濃度、乙酸和乙醇的比生成速率、CO和H2利用率和轉化率、乙酸和乙醇得率的影響等。Saxena等[25]研究了Co2+、Cu2+等微量金屬離子對C.ragsdalei的生長及乙醇產量的影響,使乙醇最大濃度達到187.8mmol/L。Guo等[26,17]采用數(shù)值方法對C.au-toethanogenum的生長培養(yǎng)基進行了優(yōu)化,并將此優(yōu)化培養(yǎng)基能應用于兩步CSTRs發(fā)酵合成氣制乙醇。
Kendall等[27]就氣體壓力對菌體生長和乙醇產生的影響進行了研究。Phillips等[4]在連續(xù)攪拌反應器中利用改進培養(yǎng)基進行發(fā)酵,乙醇質量濃度達到23g/L;在原有發(fā)酵設備基礎上聯(lián)合細胞循環(huán)系統(tǒng),發(fā)酵560h后,乙醇可以達到48g/L。利用Clostridium carboxidivorans P7轉化合成氣發(fā)酵生產燃料乙醇,優(yōu)化后的最高乙醇質量濃度可以達到10g/L[28]。
Klasson等[29]用Clostridium ljungdahlii對兩步連續(xù)攪拌反應器進行改進,利用經過凈化的煤氣合成氣發(fā)酵,煤氣成分包含25%~35%的H2、40%~65%的CO、1%~20%的CO2、0~7%的CH4,乙醇和乙酸的產量比達到4∶1,乙醇質量濃度接近3g/L。郭穎等[30]研究了合成氣和培養(yǎng)基組分對C.autoethanogenum發(fā)酵產乙醇的影響,結果表明0.075g/L玉米漿利于合成氣乙醇發(fā)酵;適量的焦油有利于乙醇的生成,抑制乙酸的產生。低濃度的乙醇和乙酸能促進對應產物乙酸和乙醇的生成。Gad-dy等[31]的專利中使用相同的菌種和發(fā)酵設備使乙醇質量濃度達到了7g/L。Kundiyana等[32]以Clos-tridiumstrain P11為研究對象,研究發(fā)酵設備由實驗室規(guī)模到中試規(guī)模的放大,在100L發(fā)酵罐中,發(fā)酵59d時,乙醇質量濃度達到24.57g/L。
美國俄克拉荷馬州立大學生物質氣化工程實驗室主要利用農作物秸稈氣化然后生物合成燃料乙醇,并建立了一個100L的中試試驗技術平臺。
美國的Coskata公司擁有一條年產2~4.5億L的合成氣制乙醇的生產線,已于2009年10月投產。
Coskata公司通過對包括木屑、柳枝稷、玉米秸稈、城鎮(zhèn)垃圾、廢舊輪胎等各種生物質的氣化,將得到的合成氣通過過濾器后通入到發(fā)酵罐中利用微生物進行發(fā)酵,發(fā)酵液利用膜技術分離,最終的乙醇體積分數(shù)可以達到99.7%。Coskata生產工藝每消耗1t干生物質可以獲得超過400L的乙醇,擁有所使用菌種和發(fā)酵設備的專利權。所用菌種是一種梭狀芽胞桿菌,只有乙醇這一種發(fā)酵產物。美國能源部聯(lián)合美國生物工程公司(BRI)對利用生物質合成氣發(fā)酵乙醇的技術進行評估后,于2003年11月在阿肯色州建立示范工程,并于2005年末開始籌建商業(yè)化的運作裝置[33]。美國密西西比乙醇公司能夠以鋸末為氣化原料合成甲醇,已經與美國能源部合作籌建合成工廠[34]。
新西蘭LanzaTech公司是一個能夠以生物質合成氣、工業(yè)廢氣為原料生產燃料乙醇的公司,該公司將城市垃圾、工業(yè)有機垃圾、廢木料等進行氣化,使用其擁有專利權的微生物用于液態(tài)燃料的發(fā)酵,能夠利用生物質中90%以上的能量。LanzaTech計劃先在2011年建立一個商業(yè)化前期工廠,隨后迅速將規(guī)模擴展為年產超過2億L的商業(yè)化工廠。2010年,河南煤化集團和中國科學院生物局、新西蘭LanzaTech公司聯(lián)合簽署協(xié)議,利用煤炭氣化生物發(fā)酵法來生產乙醇燃料及其他化工產品,并建立生物能源研發(fā)中心[35]。2011年3月份,寶鋼集團有限公司、中國科學院及新西蘭Lanzatech公司三方簽署合作協(xié)議,合作組建中國第一家廢氣再造的經營性企業(yè)“上海寶鋼朗澤能源有限公司”,并開始實施300t乙醇示范工廠項目,如示范工廠項目成功,再適時啟動10萬t/a的商業(yè)化乙醇工廠項目,實現(xiàn)產業(yè)化發(fā)展,在全國其他鋼廠推廣[36]。
3.4AT制乙醇的優(yōu)勢
合成氣厭氧發(fā)酵生產乙醇是一項極具潛力與競爭力的技術,對它的研究日益受到人們的重視[37-38]。合成氣AF法制乙醇可能會成為一項“革命性”的技術而得到世人的認可和應用。
與FT法制乙醇途徑相比,合成氣AF法制乙醇工藝更具優(yōu)勢,主要表現(xiàn)在以下方面。
1)AF法可以在環(huán)境溫和與常壓下進行,降低了能耗和設備成本,降低了生產成本,增強了生產的安全性[31]。AF法與FT法生產成本比較見表1。

2)微生物轉化法的產率要比化學轉化高出很多,因為微生物只利用底物的很少一部分來維持自身的能量需要和生長[31];
3)微生物轉化法選擇性較高,減少了發(fā)酵副產物的產生,在適宜的條件下,通過微生物發(fā)酵高選擇性地利用合成氣,減少副產物產生,得到單一乙醇產品,降低了純化成本[1];微生物的代謝過程,實際上是代謝途徑中關鍵酶的作用,而酶的重要特點之一就是底物的專一性,這就決定了微生物合成氣轉化的高度選擇性,從而可以獲得較為單一的乙醇產品;
4)微生物轉化法具有不可逆性,可以避開熱動力學平衡的限制從而實現(xiàn)較高的轉化率[39];
5)生物質合成氣的流量與合成氣中各成分的比例對乙醇合成過程的影響不大[23];和其他的合成氣反應過程相比,合成氣微生物發(fā)酵過程不需要嚴格的H2和CO的比例,菌體雖然偏好CO,但是CO和H2/CO的混合物幾乎能夠同時被轉化;
6)微生物對硫化物耐受,不會產生硫化物中毒現(xiàn)象。當硫化物(H2S、COS等)氣體體積分數(shù)為2.0%時,對發(fā)酵過程的影響很小,達到5.2%時會延緩反應,超過10%時將完全抑制細胞生長和CO的利用。一般的合成氣中,硫化物含量很小,反應過程發(fā)生中硫化物中毒的程度很輕[1,40-41];
7)生物催化劑——微生物細胞可以回收和再生,生物利用效率高,環(huán)境污染排放少[1]。
4合成氣厭氧發(fā)酵(AF)生產乙醇存在問題及建議
合成氣AF法制乙醇具有顯著的優(yōu)點,也具有巨大的發(fā)展?jié)摿Γ斍霸擃I域的研究主要存在的問題有以下幾方面。
1)可以轉化合成氣生產乙醇的微生物種類還偏少,真正能夠工業(yè)化應用的微生物菌株更少;
2)雖然人們了解了微生物利用合成氣厭氧發(fā)酵產乙醇的代謝過程,但對于合成氣厭氧發(fā)酵制取乙醇的一些關鍵性基礎問題還知之甚少,如乙醇代謝合成中受哪些因子調控,合成乙醇途徑的關鍵代謝節(jié)點及控制基因有哪些,高選擇性乙醇合成的調控機制是什么等等;
3)原料合成氣轉化率低、乙醇產物濃度低,致使乙醇生產成本較高,無法達到工業(yè)化生產和商業(yè)化運行的要求。
為了盡快實現(xiàn)以合成氣為原料通過厭氧發(fā)酵(AF)技術來生產乙醇技術的產業(yè)化,需要加強有關研究的基礎微生物學、發(fā)酵關鍵技術研究及發(fā)酵過程調控及工程化應用技術與裝備研究,實現(xiàn)技術和基礎研究的突破,推進該領域研究。
參考文獻:
[1]李東,袁振宏,王忠銘,等.生物質合成氣發(fā)酵生產乙醇技術的研究進展[J].可再生能源,2006,126:57-61.
[2]US Department of Energy,Office of the Biomass Program.Biomass program multi-year technical plan M].Washington,D.C.:[s.n.],2003.
[3]王鵬,王憲貴,郭戰(zhàn)英,等.合成氣合成乙醇的研究進展[J].潔凈煤技術,2010(1):5-62.
[4]Phillips J R,Clausen E C,Gaddy J L,et al.Biological production of ethanol from coal synthesis gas[J].Appl Biochem Biotechnol,1993,39-40(1):559-571.
[5]Maschio G,Lucchesi A,Stoppato G.Production of syngas from bi-omass[J].Bioresour Technol,1994,48(2):119-126.
[6]覃國軍.石油石化企業(yè)面臨的低碳發(fā)展挑戰(zhàn)和機遇[J].油氣田環(huán)境保護,2010,20(1):1-4.
[7]Zhu Xiangxue,Chen Fucun,An Jie,et al.Development and in-
dustrialization of the ethylbenzene production technologies from dilute ethylene in FCC dry gas[J].Adv Mats Res,2011,233-235:1708-1713.
[8]王連中,姜國生,王蘭成.煉廠干氣回收烴類作為乙烯裝置原料的可行性論證[J].化工設計,2004,14(2):43-45.
[9]藍平,藍麗紅,謝濤,等.生物質合成氣制備及合成液體燃料研究進展[J].化學世界,2011(7):437-441.
[10]士麗敏,儲偉,劉增超.合成氣制低碳醇用催化劑的研究進展[J].化工進展,2011,30(1):162-166.
[11]Haider M A,Gogate M R,Davis R J.Fe-promotion of supported Rh catalysts for direct conversion of syngas to ethanol[J].J Catal,2009,261(1):9-16.
[12]寇元.合成氣催化轉化的綠色化學[J].催化學報,2008,29(9):817-822.
[13]Kharas K,Durand J P.Cobalt-molybdenum sulfide catalyst mate-rials and methods for ethanol production from syngas:US,20090069609[P].2009-03-12.
[14]Barik S,Prieto S,Harrison S B,et al.Biological production of al-cohols from coal through indirect liquefaction[J].Appl Biochem Biotechnol,1988,18(1):363-378.
[15]Abrini J,Naveau H,Nyns E J.Clostridium autoethanogenum sp.nov.,an anaerobic bacterium that produces ethanol from carbon monoxide[J].Arch Microbiol,1994,161(4):345-351.
[16]Rajagopalan S,Datar R P,Lewis R S.Formation of ethanol from carbon monoxide via a new microbial catalyst[J].Biomass Bioen-ergy,2002,23(6):487-493.
[17]郭穎,許敬亮,徐惠娟,等.Clostridium autoethanogenum的生長培養(yǎng)基優(yōu)化[J].可再生能源,2011,29(1):53-56.
[18]張?zhí)m波,劉繼開,李東,等.合成氣乙醇發(fā)酵的微生物研究[J].可再生能源,2007,25(3):27-30.
[19]Hurst K M,Lewis R S.Carbon monoxide partial pressure effects on the metabolic process of syngas fermentation[J].Biochem Eng J,2010,48(2):159-165.
[20]Kpke M,Held C,Hujer S,et al.Clostridium ljungdahlii repre-sents a microbial production platform based on syngas[J].PNAS,2010,107(29):13087-13092.
[21]Wilkins M R,Atiyeh H K.Microbial production of ethanol from carbon monoxide[J].Curr Opin Biotech,2011,22(3):326-330.
[22]Abubackar H N,Veiga M C,Kennes C.Biological conversion of carbon monoxide:rich syngas or waste gases to bioethanol[J].Biofuels,Biopro Bioref,2011,5(1):93-114.
[23]Munasinghe P C,Khanal S K.Biomass-derived syngas fermenta-tion into biofuels:opportunities and challenges[J].Bioresour Technol,2010,101(13):5013-5022.
[24]Klasson K T,Ackerson C M D,Clausen E C,et al.Bioreactor de-sign for synthesis gas fermentations[J].Fuel,1991,70 (9):605-614.
[25]Saxena J,Tanner R S.Effect of trace metals on ethanol production from synthesis gas by the ethanologenic acetogen,Clostridium ragsdalei[J].J Ind Microbiol Biotechnol,2011,38(4):513-521.
[26]Guo Y,Xu J,Zhang Y,et al.Medium optimization for ethanol produc-tion with Clostridium autoethanogenum with carbon monoxide as sole carbon source[J].Bioresour Tech,2010,101(22):8784-8789.
[27]Kendall M H,Randy S L.Carbon monoxide partial pressure
effects on the metabolic process of syngas fermentation[J].Bio-chem Eng J,2010,48(2):159-165.
[28]Liou J C,Balkwill D L,Drake G R,et al.Clostridium carboxidi-vorans sp.nov.,a solvent-producing Clostridium isolated from an agricultural settling lagoon,and reclassification of Clostridium scatologenes strain SL1 as Clostridium drakei sp.nov.[J].Int J Syst Evol Microbiol,2005(55):2085-2091.
[29]Klasson K T,Ackerson C M D,Clausen E C,et al.Biological con-version of synthesis gas into fuels[J].Int Assoc Hydrogen Ener-gy,1992,17(4):281-288.
[30]郭穎,許敬亮,徐惠娟,等.合成氣和培養(yǎng)基組分對 C.autoeth-
anogenum 發(fā)酵產乙醇的影響研究[J].太陽能學報,2011,32(9):1370-1374.
[31]Gaddy J L,Clausen E C.Clostridium ljungdahlii an anaerobic ethanol and acetate producing microorganism:US,5173429[P].1992-12-22.
[32]Kundiyana D K,Huhnke R L,Wilkins M R.Syngas fermentation
in a 100-L pilot scale fermentor:design and process considera-tions[J].J Biosci Bioeng,2010,109(5)492-498.
[33]李東,袁振宏,呂鵬梅,等.合成氣生物利用的研究進展[J].生物質化學工程,2007,41(2):54-58.
[34]閆強,王安建,王高尚.全球生物質能源評價[J].中國農學通報,2009,25(18):466-470.
[35]中華網(wǎng).攜手中科院新西蘭 LanzaTeck 公司,河南煤業(yè)化工集團公司進軍清潔能源領域[N/OL].[2011-12-10].http://henan.china.com/zh_cn/finance/pinpai/11084294/20100907/16130237.html.
[36]金融界.寶鋼聯(lián)手中科院等合作探索鋼廠尾氣制乙醇新技術[N/OL].[2011-12-10].http://finance.jrj.com.cn/industry/2011/03/2809239577373.shtml.
[37]徐惠娟,許敬亮,郭穎,等.合成氣厭氧發(fā)酵生產有機酸和醇的研究進展[J].中國生物工程雜志,2010,30(3):112-118.
[38]宋安東,馮新軍,謝慧,等.生物質合成氣發(fā)酵制取燃料乙醇研究進展[J].食品與發(fā)酵工業(yè),2011,37(6):130-136.
[39]Grethlen A J,Mahendra.Bioprocessing of coal-derived synthesis gases by anaerobic bacteria[J].Trends Biotech,1992,10 (12):418-423.
[40]Grethlen A J,Sonib K,Worden R M,et al.Influence of hydrogen sulfide on the growth and metabolism of Butyribacterium methyl-otrophicum and Clostridium acetobutylicum[J].J Appl Biochem,1992,34-35(1):233-246.
[41]Vega J L,Klasson K T,Kimmel D E,et al.Sulfur gas tolerance and toxicity of CO-utilizing and methanogenic bacteria[J].Appl Biochem Biotechnol,1990,24-25(1):329-340. |
